题记:
自然规律在高维空间表述时会变得更为简单和优美。
——《超越时空》

二元悖论
新的技术平台能够解锁新的认知边界,新的认知能够催生新技术。高通量测序(NGS)技术的出现为大规模解析肿瘤基因组信息提供了可能,同时分子表达谱技术使得对整块混合组织的基因表达获得前所未有的信息量。单细胞测序技术一定程度上加深了对组织中不同细胞类型及同类型细胞的亚群之间遗传异质性的理解。原位可视化技术如标准的免疫组织化学(IHC)染色和荧光原位杂交(FISH)可以获得单个蛋白的组织原位表达信息。
然而,在当前的每一次组织分析时,研究人员都需要在形态成像技术和高通量分析技术间进行两难选择,在信息维度、通量、分辨率和精密度之间做出取舍。在免疫肿瘤学研究中,这一悖论引发的局限性尤其明显。肿瘤在不同样本中的结构、(免疫)细胞组成、丰度和分布方面具有高度异质性,其所导致的肿瘤微环境的复杂性是当前肿瘤免疫研究和转化医学所面临的的重大挑战。
而基于当前研究手段转化出的结果应用到临床上,用于指导患者用药或提示预后时,总会遇到这样那样的问题。如下图所示,两位患者进行了基于传统基因表达检测技术的,其TIS(Tumor Inflammation Signature)评分相近,但临床预后存在着明显的差异,经过mIF技术进行空间可视化标记后才发现其肿瘤组织内部免疫细胞的浸润程度有明显区别,肿瘤内异质性差异较大。肿瘤免疫研究中空间信息的重要性已经日益显现。
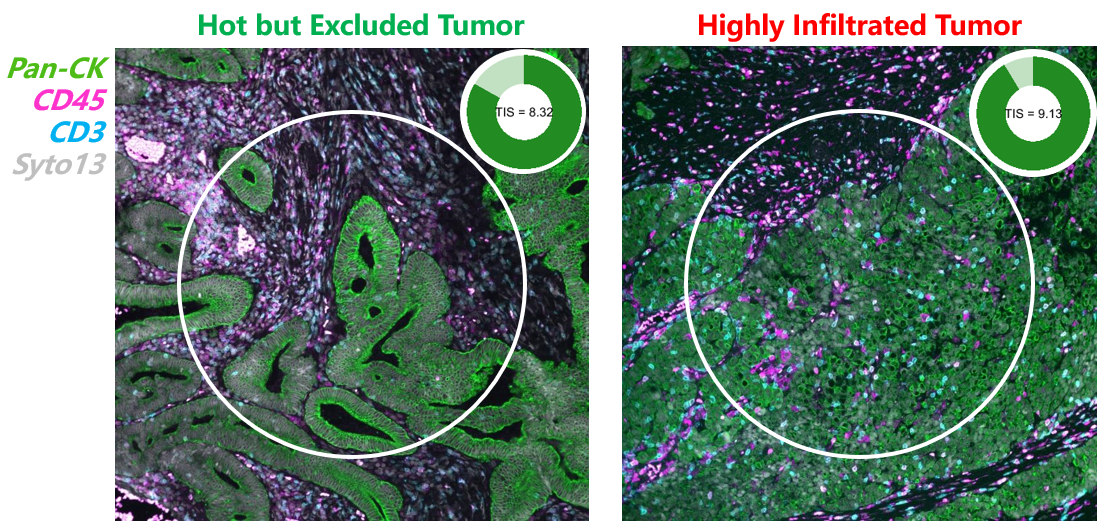
从混合物研究,升级到三维的空间
我们希望通过解析肿瘤区域内免疫细胞亚群的详细表征以提高我们对抗肿瘤免疫和对免疫检查点抑制剂抵抗的理解,基于整块混合组织的RNA表达数据的聚类分析或许可以获得免疫细胞的分类和相对定量,然而却要以牺牲重要的空间信息作为代价。我们还需要了解肿瘤和免疫细胞共定位,以加深对于生物标志物的理解和识别,最终实现精准免疫治疗。肿瘤微环境的复杂性要求单张组织样本切片产出多重信息,提高对于样本切片特别是珍贵样本的利用率。多色免疫荧光(mIF)利用TSA技术(Tyramide Signal Amplification)利用辣根过氧化酶(HRP)对靶蛋白进行高密度原位标记,使得单张切片的研究靶标数可以多至6个。相比于标准的IHC染色不仅节约了样本,还能实现多靶标双阳分析、免疫分型、细胞间距离分析、三级淋巴结构分析(TLS)等。
而如何在组织样本中进行区域化和定量化蛋白质和RNA的特征分析也被证实具有挑战性。2019年发布的GeoMx DSP技术可在同一临床样本中的多个感兴趣区域(ROI)一次性测定多达上百个蛋白,或1833个RNA靶标或全转录组,同时实现保留空间原位信息前提下的高参数、多组学、高精度研究。以GeoMx DSP为代表的空间多组学技术被评为Nature Methods 2020年度技术和Nature 2022年七大颠覆性技术。

从三维的空间,升级为四维的时空
古希腊哲学家赫拉克利特曾说过:“人不能两次踏入完全相同的河流。”河流奔涌向前的过程中,水早已不是原来的水了。世界上的万事万物,永远都处于不停变幻中,肿瘤当然也不例外。肿瘤的进化无异于一部人类进化史的缩影,肿瘤细胞在分裂增殖中会不断累积体细胞突变,在环境压力(治疗、人体免疫系统、肿瘤微环境)下,其中一些突变会给肿瘤细胞带来更强的适应性优势,逃离人体免疫系统的监视,带来耐药、复发、转移的终极难题。在屡战屡败中我们获得的教训是,单点的信息不足以指导这场对抗肿瘤的持久战,只有基于动态、多点地监测信息不断调整对抗策略才能获得更高的胜率。
外周循环系统中蕴涵着大量的过程信息,血液样本通过非侵入性方式采集,相对组织更易于获取,利于多次检测。循环肿瘤DNA(ctDNA)可以表征肿瘤基因组特征(突变、数量、异质性)和评估微小残留病灶(定量数值),可以提示预后并指导下一步治疗策略制定。包括血清癌胚抗原、甲胎蛋白在内的循环蛋白质是当前临床上常用的肿瘤标志物,用免疫学,生物学以及化学的方法来检测到,但受到灵敏度、通量的局限限制。Olink独有的邻位延伸分析(PEA)技术,将蛋白浓度信号转换成核酸信号,从而实现飞克级、3000多重的蛋白检测,打破传统蛋白检测的技术壁垒,轻松实现微量血浆样本的高通量、高灵敏度的蛋白质组学检测。在准确检出高丰度蛋白的同时,也不会错过具有生物标志物潜能的低丰度蛋白。
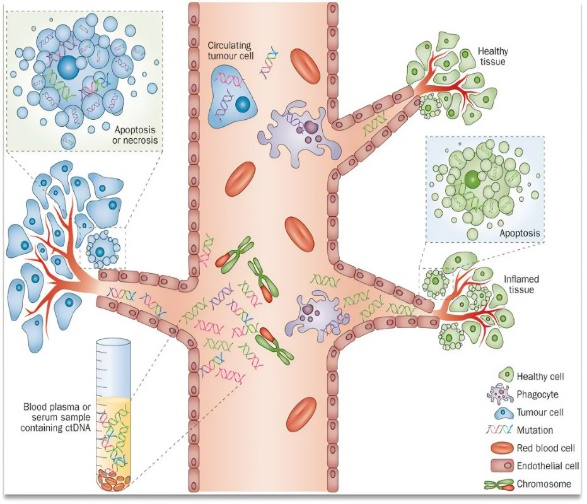
定义肿瘤免疫时空组学
太阳集团tyc官方入口深耕肿瘤免疫领域近七载,不断在“让肿瘤免疫更有效”方向上寻求本质解。通过自身大量科研实践,对于肿瘤免疫的复杂性和传统研究方法的局限性有着深刻的理解。随着研究的深入和技术平台不断发展,太阳集团tyc官方入口从肿瘤基因组和肿瘤微环境两个角度对多维技术平台进行了前瞻性的布局。

在空间和时间维度引入更多平台之间的协作,并提出肿瘤免疫时空组学的概念,即通过对多平台多维度的创新研究方法进行整合,实现肿瘤免疫研究的“空间聚焦”和“动态检测”,通过临床可及的样本一站式获取高通量、高精密度、空间原位、多重数、多时点监测数据。
在空间维度,借助空间转录组、空间蛋白组、多色免疫荧光等技术来解析肿瘤微环境空间层面的信息,使抗肿瘤免疫反应主战场上的战况清晰可见。
在时间维度,借助单细胞测序、循环蛋白质组学检测以及ctDNA NGS检测技术来解析不同时间点的肿瘤基因组特征信息和细胞间通讯,建立抗肿瘤免疫的情报系统。
太阳集团tyc官方入口通过组建这套国内独有、国际前沿的为肿瘤免疫方向量身定制的时空组学科研平台,助力研究思路的开拓,研究水平的提升,把对肿瘤免疫的认知升维到前所未有的新境界,并通过转化医学最终实现临床应用,让肿瘤免疫治疗更精准有效,让更多患者获益。
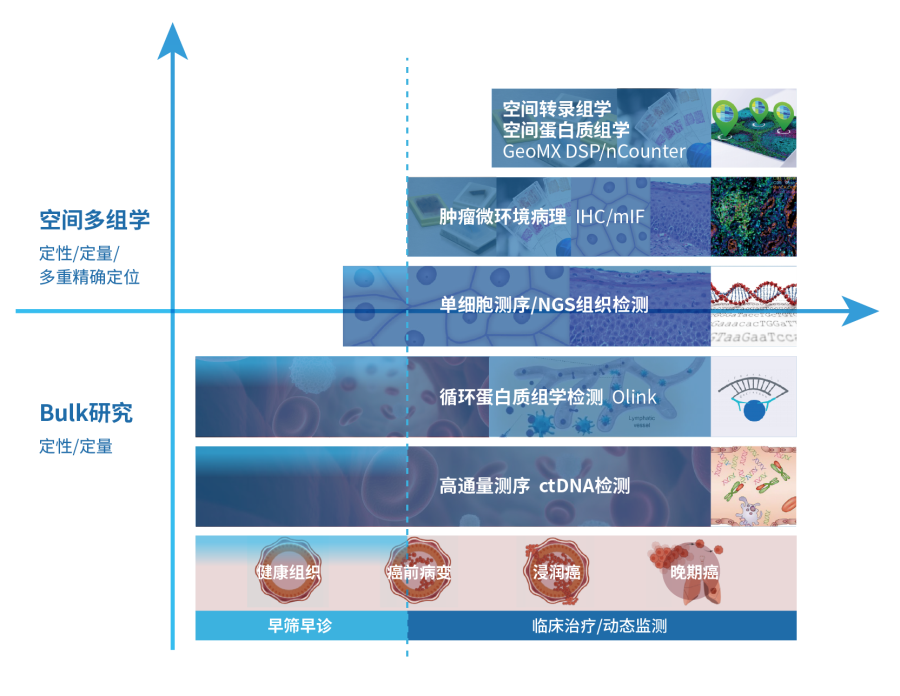
共同实践验证未来发展方向
多平台多维度的整合创新性研究方法,在当前的肿瘤免疫研究中已经成为一种趋势,随着越来越多的研究成果得到发表,进一步印证了“肿瘤免疫时空组学”这一概念的可行性。
Case 1
乔治敦大学医院研究团队利用NanoString的GeoMx® Digital Spatial Profiler (DSP)技术和NanoString nCounter PanCancer IO 360™(IO 360)检测Panel,对多个HER2+乳腺癌患者的原发灶和转移灶的TME进行分析,以了解在HER2+乳腺癌患者的诊疗过程中肿瘤复发或转移后的免疫微环境变化。
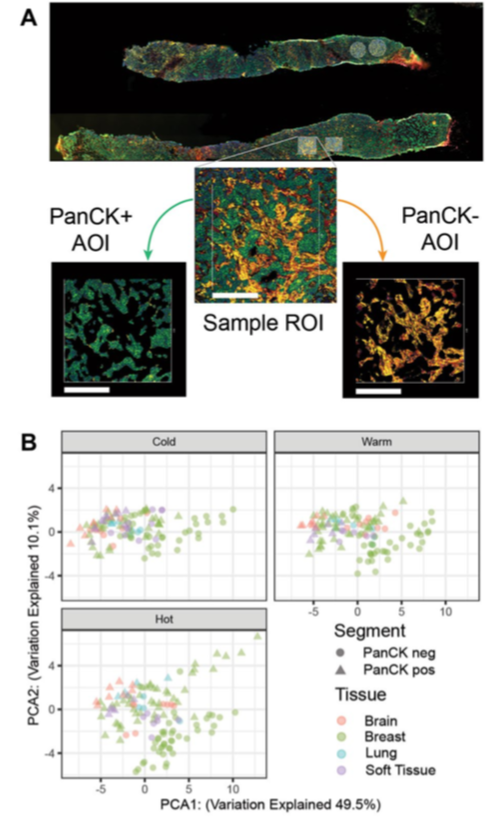
Citation:Schlam I, et al. The tumor immune microenvironment of primary and metastatic HER2- positive breast cancers utilizing gene expression and spatial proteomic profiling. J Transl Med. 2021 Nov 27;19(1):480. doi: 10.1186/s12967-021-03113-9.
详细解读:《文献解读|空间蛋白组学助力乳腺癌肿瘤微环境研究》
Case 2
MIT和哈佛大学Broad研究所的知名生物信息专家Aviv Regev团队利用单细胞RNA测序 (scRNA-seq)、NanoString的GeoMx Digital Spatial Profiler (DSP)以及遗传和药理学干扰技术对SyS的免疫微环境和空间生态系统进行研究,揭示了免疫逃逸和致癌过程之间的相互作用,并针对 SyS 提出了潜在的新治疗策略。
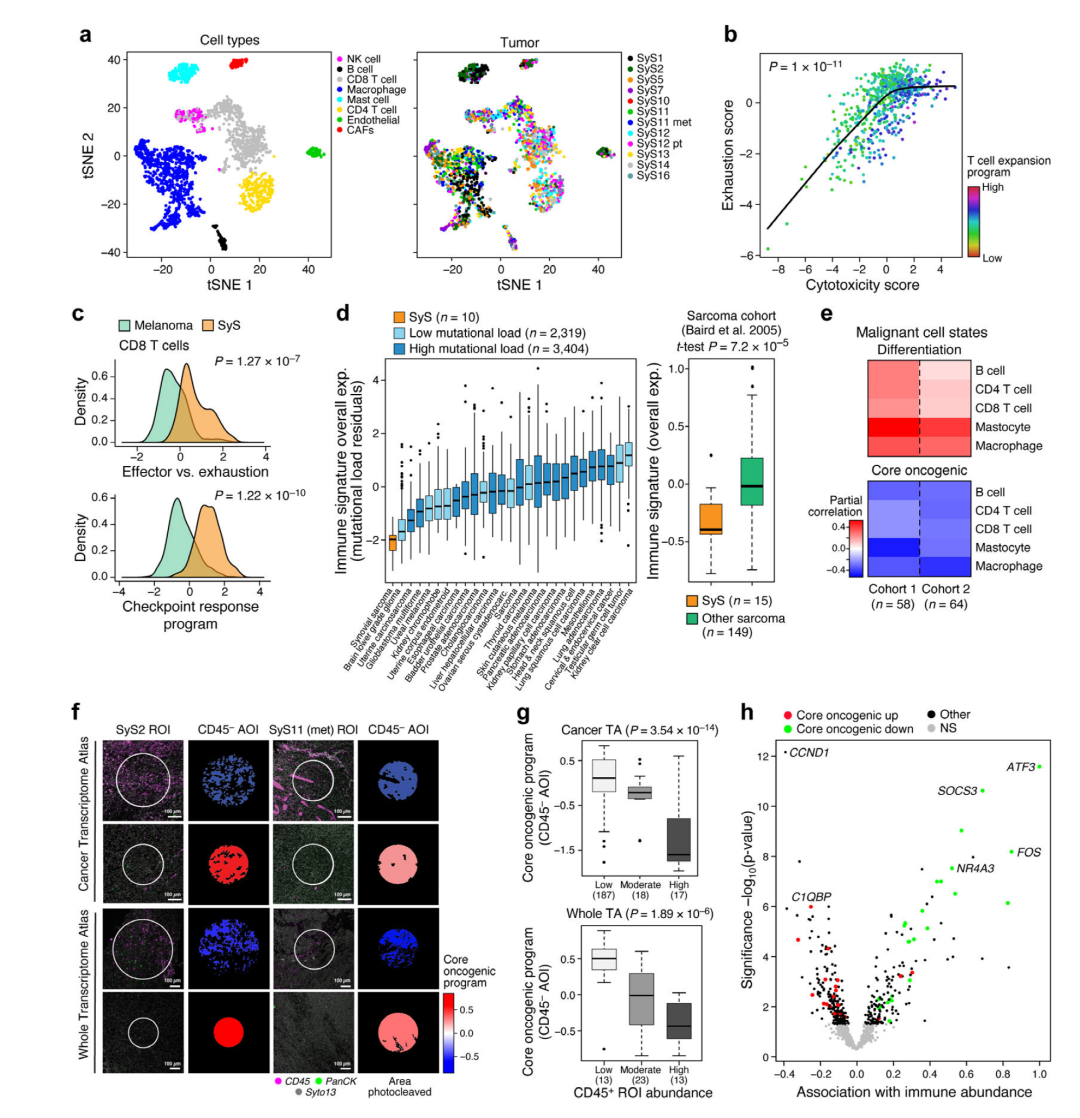
Citation:Jerby-Arnon L, et al. Opposing immune and genetic mechanisms shape oncogenic programs in synovial sarcoma. Nat Med. 2021 Feb;27(2):289-300. doi: 10.1038/s41591-020-01212-6.
详细解读:《文献解读|空间转录组联合单细胞测序技术揭秘滑膜肉瘤核心致癌程序》
Case 3
麻省理工学院团队从胰腺癌特异性新抗原出发,在胰腺癌中发现了功能类似于PD-1/PD-L1的刹车系统—CD155/TIGIT会导致PDAC免疫逃逸。在临床前小鼠模型中开发了一种免疫治疗策略—PD-1抑制剂+TIGIT抑制剂+CD40激动剂,可以消除小鼠的胰腺肿瘤,为胰腺癌免疫治疗带来新希望。研究者应用空间蛋白组技术结合单细胞测序等多种技术,从组织空间等多角度深刻阐释了该策略背后的分子机制。
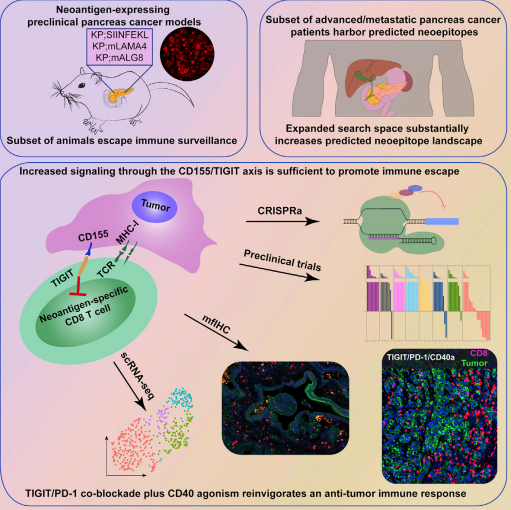
Citation:Freed-Pastor WA, et al. The CD155/TIGIT axis promotes and maintains immune evasion in neoantigen-expressing pancreatic cancer. Cancer Cell. 2021 Oct 11;39(10):1342-1360.e14. doi: 10.1016/j.ccell.2021.07.007.
详细解读:《文献解读|空间蛋白组联合单细胞测序技术揭秘胰腺癌免疫逃逸新机制》
Case 4
耶鲁大学医学院病理学系教授David L. Rimm 团队联合NanoString科技公司应用空间蛋白组(GeoMx® DSP) 结合多色免疫荧光 (mIF) 技术在NSCLC中探究对PD-1检查点抑制剂响应的生物标志物。研究结果证实基质区高密度的CD56+免疫细胞的患者有更久的无进展生存期(PFS)及总生存期(OS) 相关。
此项中试规模的发现队列展示了基于DSP和nCounter平台的空间蛋白组学研究联合mIF技术在NSCLC中鉴定对PD-1检查点抑制剂响应的空间相关生物标志物的应用潜力。
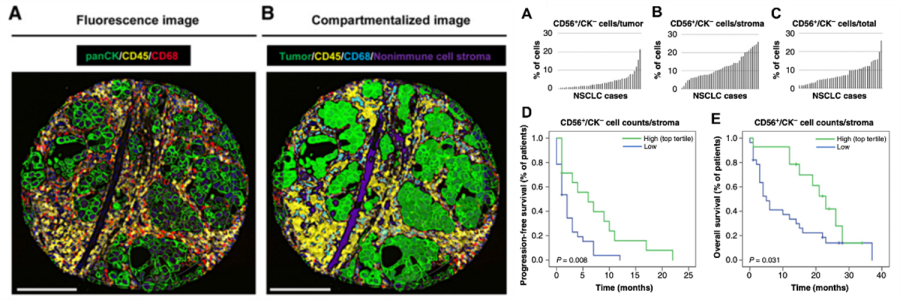
Citation: Zugazagoitia J, et al. Biomarkers Associated with Beneficial PD-1 Checkpoint Blockade in Non-Small Cell Lung Cancer (NSCLC) Identified Using High-Plex Digital Spatial Profiling. Clin Cancer Res. 2020 Aug 15;26(16):4360-4368. doi: 10.1158/1078-0432.CCR-20-0175.
详细解读:《文献解读|DSP+nCounter+mIF如何发表高分文章?》
Case 5
中山大学孙逸仙纪念医院刘洁琼教授团队发起的探索艾瑞布林联合卡瑞利珠单抗以及阿帕替尼治疗aTNBC患者的多中心、单臂的临床试验结果正式发表在Nature Communications(IF=14.919)。太阳集团tyc官方入口负责该研究中mIF与olink的检测及数据解析工作。该前瞻性研究证实了卡瑞利珠单抗联合阿帕替尼和艾瑞布林在既往接受过治疗的aTNBC患者中表现出良好的安全性和有效性,即使PD-L1阴性肿瘤患者或那些接受了包括免疫检查点抑制剂在内的多种不成功的全身治疗的患者,仍然可以从这种联合治疗方案中受益。

Citation: Liu J, et al. Multicenter phase II trial of Camrelizumab combined with Apatinib and Eribulin in heavily pretreated patients with advanced triple-negative breast cancer. Nat Commun. 2022 May 31;13(1):3011. doi: 10.1038/s41467-022-30569-0.
详细解读:《文章发表|多组学平台助力aTNBC免疫联合化疗及抗血管生成药物研究获得新进展》
太阳集团tyc官方入口——肿瘤免疫科研优选合作伙伴
太阳集团tyc官方入口作为肿瘤精准免疫诊疗整体解决方案提供商,致力于为肿瘤免疫领域的基础医学、临床研究和转化医学研究者提供国际前沿的临床转化科研服务。临床样本友好的基因表达谱检测、免疫微环境多重蛋白检测、高通量循环蛋白检测提供了海量、充分、多角度信息,结合强大的空间多组学分析技术,组成从生物标志物/靶点发现、验证到转化的整体解决方案,促进精准医疗和个体化治疗方案的制定、发展与实施。

Copyright©2021
太阳集团tyc官方入口 - 太阳集团游戏官方网址 版权所有
粤ICP备16128839号
