美国癌症研究协会(AACR)年会已经接近尾声,会议上发布了各种肿瘤治疗新突破,不断惊艳全场。关于PD-1抑制剂的临床研究也是与会专家学者热议的话题。太阳集团tyc官方入口和武汉协和医院合作发表的壁报(Poster)正是与之相关。

图1.AACR会议Poster展出现场
2018年8月28日百时美施贵宝欧狄沃(Opdivo)(纳武利尤单抗注射液,Nivolumabinjection)在中国上市,获批用于非小细胞肺癌(NSCLC)的二线治疗。中国非小细胞肺癌从此迈入免疫治疗新时代。NSCLC病人对免疫检测点抑制剂的应答率只有20%,有效的预后biomarker是精准免疫治疗的基础。尽管TMB是研究最为广泛的biomarker,但也有一些病人TMB水平高,却很难从免疫治疗中获益。所以,有必要进一步探索其他同疗效相关的基因组biomarker。
图2.AACR参展Poster全图
这篇Poster的研究对象是多形性肺癌,多形性肺癌属于肉瘤样肺癌,是NSCLC中的稀有亚型,恶性程度高,侵袭性强,常表现出对放化疗的耐药。尽管有临床研究发现免疫检测点抑制剂对个别多形性肺癌患者有一定疗效,但预后biomarker没有被深入研究过。
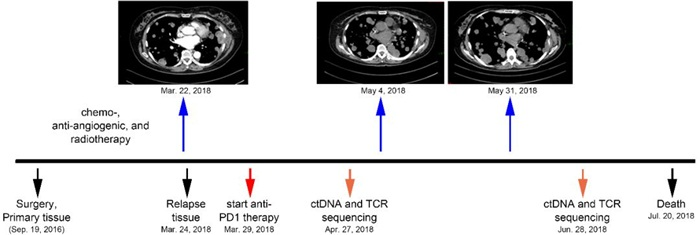
图3.患者治疗史和实验设计
一名57岁女性肺多形性癌患者接受了手术、化疗、抗血管治疗、放疗和抗PD-1药物治疗,然而病情没有得到控制,抗PD-1药物治疗4个多月后死亡。研究对原发灶和放化疗后的复发灶进行了目标区域测序(YuceOne®Plus,涵盖811个肿瘤相关基因)。另外,还收集了抗PD-1药物治疗过程中两个时间点的外周血,进行ctDNA和TCR测序,以监控免疫药物的应答情况。结果发现尽管复发灶TMB水平高(10.7/Mb),但实际上并没有从抗PD-1药物治疗中获益。随后,研究者进一步考虑瘤内异质性对免疫应答的影响,结果显示复发灶中亚克隆新抗原占比相对原发灶有显著的上升,提示放化疗产生的瘤内异质性增强可能是导致抗PD-1药物耐药的主要原因。
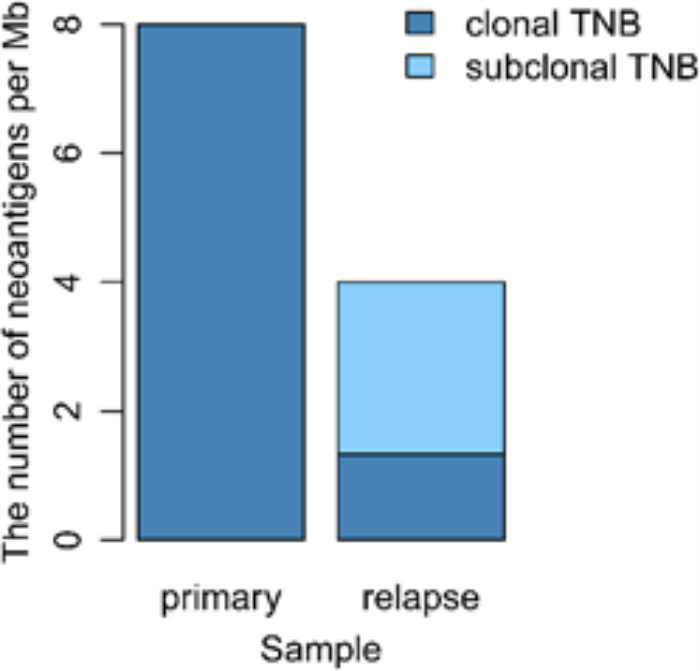
图4.原发性肿瘤和复发肿瘤的TNB分布
接下来,该研究评估了ctDNA对免疫治疗的预后监控能力,将ctDNA突变按细胞丰度聚成不同的clusters,发现ctDNA的克隆结构同组织克隆结构的相似性,ctDNA倾向于检出肿瘤组织中的克隆突变,ctDNA中突变的细胞丰度增加提示组织中对应的细胞克隆扩增。另外,ctDNA中两个克隆新抗原突变丰度在抗PD-1药物治疗过程中增加,提示组织中的克隆扩增,推测这些携带新抗原的肿瘤细胞没有被免疫系统清除。
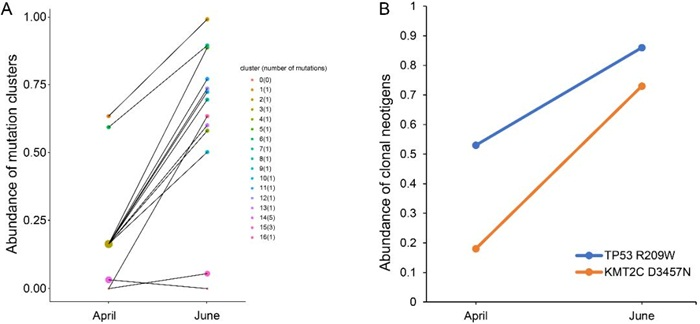
图5.免疫治疗过程中ctDNA突变丰度增加(A)、两个克隆新抗原突变丰度增加(B)
此外,研究还观察了TCR谱在抗PD-1药物治疗过程中的改变,以推断T细胞的免疫应答情况。研究发现TCR克隆频率的动态改变,大多数高频的TCR克隆在治疗过程中频率显著下降(p<0.01),提示肿瘤细胞没有有效地激活T细胞的免疫应答。
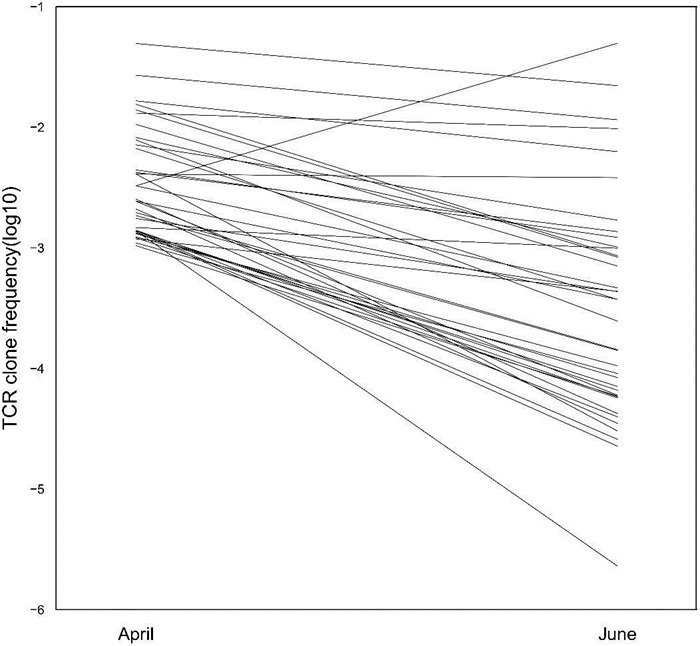
图6.免疫治疗过程中高频TCR克隆频率的变化
本研究证实了尽管TMB水平高,但放化疗诱导瘤内异质性增加对免疫药物应答产生了负面影响,提示用药前对预后的评估需要考虑这方面因素;还阐明了ctDNA联合TCR可有效监控抗PD-1药物治疗过程中机体免疫系统的特异性应答。这项研究对免疫检测点抑制剂的用药指导和预后监控有一定的参考价值。
参考文献
[1] Topalian SL, etal. Safety, activity, and immune correlates of anti-PD-1 antibody incancer. N Engl J Med. 2012 Jun 28;366(26):2443-54.
[2] Brahmer JR, etal. Safety and activity of anti-PD-L1 antibody in patients withadvanced cancer. N Engl J Med. 2012 Jun 28;366(26):2455-65.
[3] Goodman AM, etal. Tumor Mutational Burden as an Independent Predictor of Responseto Immunotherapy in Diverse Cancers. Mol Cancer Ther. 2017Nov;16(11):2598-2608.
[4] Samstein RM, etal. Tumor mutational load predicts survival after immunotherapyacross multiple cancer types. Nat Genet. 2019 Feb;51(2):202-206.
【 返回列表 】
Copyright©2021
太阳集团tyc官方入口 - 太阳集团游戏官方网址 版权所有
粤ICP备16128839号
